Electrolysis of Water
Electrolysis of water (กระบวนการอิเล็กโทรไลซิสของน้ำ) เป็นกระบวนการแยกอะตอมของน้ำ ออกเป็นก๊าซไฮโดรเจนและก๊าซออกซิเจน โดยใช้ไฟฟ้า
2H2O + พลังงานไฟฟ้า ![]() O2 + 2H2
O2 + 2H2 
'I propose to distinguish these bodies by calling those anions which go to the anode ....and those passing to the cathode, cations '
Michael Faraday 1834
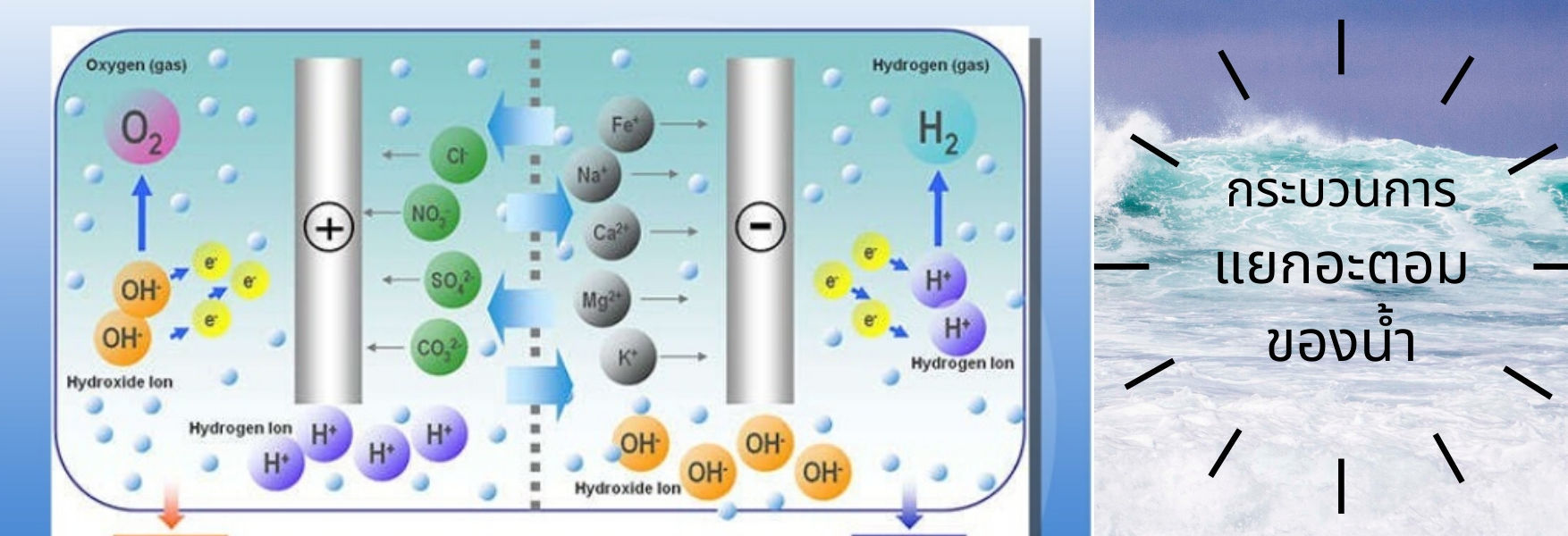
การผ่านกระแสไฟฟ้าลงไปในน้ำ จะทำให้แร่ธาตุที่มีประจุบวก รวมทั้ง hydrogen ions (H3O+) ที่เกิดจากการแตกตัวของน้ำ เคลื่อนที่ไปที่แผ่นเพลตขั้วลบ (negative electrode - cathode) และ แร่ธาตุที่มีประจุลบ รวมทั้ง hydroxide ions (OH-)ที่เกิดจากการแตกตัวของน้ำ เคลื่อนที่ไปที่แผ่นเพลตขั้วบวก (positive electrode - anode) หากมีพลังงานไฟฟ้ามากเพียงพอ จะเกิดกระบวนการอิเล็กโทรไลซิส ได้เป็นก๊าซออกซิเจน เกิดขึ้นที่ขั้วบวก และก๊าซไฮโดรเจน เกิดขึ้นที่ขั้วลบ โดย
กระบวนการอิเล็กโทรไลซิสของน้ำนั้น จะต้องมีแร่ธาตุอยู่ด้วย ดังนั้น น้ำ RO จึงไม่สามารถเกิดกระบวนการอิเล็กโทรไลซิสของน้ำได้
| Anode | +ve | 6H2O(l) |
| Cathode | -ve | 4e-(from cathode) + 4H2O(l) |
| Overall |
2H2O(l) |
|